Строение атома
Содержание:
Электронные формулы элементов первых четырех периодов
Рассмотрим заполнение электронами оболочки элементов первых четырех периодов. У водорода заполняется самый первый энергетический уровень, s-подуровень, на нем расположен 1 электрон:
+1H 1s1 1s
У гелия 1s-орбиталь полностью заполнена:
+2He 1s2 1s
Поскольку первый энергетический уровень вмещает максимально 2 электрона, у лития начинается заполнение второго энергетического уровня, начиная с орбитали с минимальной энергией — 2s. При этом сначала заполняется первый энергетический уровень:
+3Li 1s22s1 1s 2s
У бериллия 2s-подуровень заполнен:
+4Be 1s22s2 1s 2s
Далее, у бора заполняется p-подуровень второго уровня:
+5B 1s22s22p1 1s 2s 2p
У следующего элемента, углерода, очередной электрон, согласно правилу Хунда, заполняет вакантную орбиталь, а не заполняет частично занятую:
+6C 1s22s22p2 1s 2s 2p
Попробуйте составить электронную и электронно-графическую формулы для следующих элементов, а затем можете проверить себя по ответам конце статьи:
5. Азот
6. Кислород
7. Фтор
У неона завершено заполнение второго энергетического уровня:
+10Ne 1s22s22p6 1s 2s 2p
У натрия начинается заполнение третьего энергетического уровня:
+11Na 1s22s22p63s1 1s 2s 2p 3s
От натрия до аргона заполнение 3-го уровня происходит в том же порядке, что и заполнение 2-го энергетического уровня. Предлагаю составить электронные формулы элементов от магния до аргона самостоятельно, проверить по ответам.
8. Магний
9. Алюминий
10. Кремний
11. Фосфор
12. Сера
13. Хлор
14. Аргон
А вот начиная с 19-го элемента, калия, иногда начинается путаница — заполняется не 3d-орбиталь, а 4s. Ранее мы упоминали в этой статье, что заполнение энергетических уровней и подуровней электронами происходит по энергетическому ряду орбиталей, а не по порядку. Рекомендую повторить его еще раз. Таким образом, формула калия:
+19K 1s22s22p63s23p64s11s 2s 2p3s 3p4s
Для записи дальнейших электронных формул в статье будем использовать сокращенную форму:
+19K 4s1 4s
У кальция 4s-подуровень заполнен:
+20Ca 4s2 4s
У элемента 21, скандия, согласно энергетическому ряду орбиталей, начинается заполнение 3d-подуровня:
+21Sc 3d14s2 4s 3d
Дальнейшее заполнение 3d-подуровня происходит согласно квантовым правилам, от титана до ванадия:
+22Ti 3d24s2 4s 3d
+23V 3d34s2 4s 3d
Однако, у следующего элемента порядок заполнения орбиталей нарушается. Электронная конфигурация хрома такая:
+24Cr 3d54s1 4s 3d
В чём же дело? А дело в том, что при «традиционном» порядке заполнения орбиталей (соответственно, неверном в данном случае — 3d44s2) ровно одна ячейка в d-подуровне оставалась бы незаполненной. Оказалось, что такое заполнение энергетически менее выгодно. А более выгодно, когда d-орбиталь заполнена полностью, хотя бы единичными электронами. Этот лишний электрон переходит с 4s-подуровня. И небольшие затраты энергии на перескок электрона с 4s-подуровня с лихвой покрывает энергетический эффект от заполнения всех 3d-орбителей. Этот эффект так и называется — провал или проскок электрона. И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
У следующих элементов «традиционный» порядок заполнения орбиталей снова возвращается. Конфигурация марганца:
+25Mn 3d54s2
Аналогично у кобальта и никеля. А вот у меди мы снова наблюдаем провал (проскок) электрона — электрон опять проскакивает с 4s-подуровня на 3d-подуровень:
+29Cu 3d104s1
На цинке завершается заполнение 3d-подуровня:
+30Zn 3d104s2
У следующих элементов, от галлия до криптона, происходит заполнение 4p-подуровня по квантовым правилам. Например, электронная формула галлия:
+31Ga 3d104s24p1
Формулы остальных элементов мы приводить не будем, можете составить их самостоятельно и проверить себя в Интернете.
Некоторые важные понятия:
Внешний энергетический уровень — это энергетический уровень в атоме с максимальным номером, на котором есть электроны. Например, у меди (3d104s1) внешний энергетический уровень — четвёртый.
Валентные электроны — электроны в атоме, которые могут участвоват ьв образовании химической связи. Например, у хрома (+24Cr 3d54s1) валентными являются не только электроны внешнего энергетического уровня (4s1), но и неспаренные электроны на 3d-подуровне, т.к. они могут образовывать химические связи.
5.
Фотон
Представьте себе луч желтого солнечного света, сияющего через окно. Согласно квантовой физике, этот луч состоит из миллиардов крошечных пакетов света, называемых фотонами, которые текут по воздуху. Но что такое фотон?
Фотон – это наименьшее дискретное количество или квант электромагнитного излучения. Это основная единица всего света.
Фотоны всегда находятся в движении и в вакууме движутся с постоянной скоростью всем наблюдателям 2,998 × 10 8 м/с. Обычно это называют скоростью света, обозначаемой буквой с.
Согласно квантовой теории света Эйнштейна, фотоны имеют энергию, равную частоте их колебаний, умноженной на постоянную Планка. Эйнштейн доказал, что свет – это поток фотонов, энергия этих фотонов – это высота частоты их колебаний, а интенсивность света соответствует количеству фотонов.
Электроны и электричество
Электричество – это поток электронов через проводник, обычно в виде проволоки, этот поток называется электрическим током.
Чтобы этот поток произошел, электроны должны разорвать свою атомную связь (электричество – это поток электронов, а не их поток с ядрами, с которыми они связаны). Разрыв атомной связи между электроном и его ядром требует ввода энергии, которая заставляет электрон преодолевать электромагнитную силу, сдерживающую его, и таким образом свободно течь.
Проводящий материал
Все формы материи содержат электроны, однако в некоторых материалах они более свободно связаны с их ядрами. Эти материалы (известные как проводники или металлы) требуют очень мало энергии для создания электрического тока, потому что слабо связанные электроны требуют гораздо меньше энергии для преодоления электромагнитной силы, удерживающей их на месте.
Что генерирует поток электронов?
Поток электронов можно генерировать различными способами, но основные из них следующие:
- Электрические генераторы – это устройства, использующие принцип электромагнитной индукции. Электромагнитная индукция это процесс перемещения проводника через магнитное поле с целью создания электронного потока. Требуется только относительное движение проводника и магнитного поля, что означает, что магнитное поле может двигаться, пока проводник неподвижен. Когда электроны в проводнике проходят через магнитное поле (если поле достаточно сильное, а относительная скорость проводников через поле достаточно быстрая), то связи с их ядрами будут разорваны и будет индуцирован поток. Для того чтобы вызвать высокий уровень электронного потока, необходимо большое количество энергии для создания относительной скорости между проводником и магнитами.
- Химические реакции внутри батарей также создают электродвижущую силу, заставляющую электроны течь по цепи.
- Фотоны (энергия света) также могут вызывать поток электронов, когда они сталкиваются с фотоэлектрической ячейкой расположенной в солнечной панели.
Таким образом, структура или состав атома определяет принадлежность к тому или иному химическому элементу.
Шаги
Метод 1 из 2:
Определение числа нейтронов в атомах (не изотопах)
1
Найдите элемент в периодической таблице. Для примера мы будем рассматривать осмий (Os), который находится в шестом периоде (шестой ряд сверху).
2
Найдите атомный номер элемента. Это, как правило, наиболее заметное число в ячейке элемента и обычно находится над его символом (в варианте периодической системы, которую мы используем в нашем примере, других номеров и нет). Атомный номер — это количество протонов в одном атоме этого элемента.Число протонов неизменно, именно оно и делает элемент элементом. Для осмия это число 76, то есть в одном атоме осмия содержится 76 протонов.
3
Найдите атомную массу элемента. Это число обычно находится под символом элемента
Обратите внимание, что в варианте периодической системы в нашем примере атомная масса не приведена (это не всегда так; во многих вариантах периодической системы атомная масса указана). Атомная масса осмия — 190,23.
4
Округлите атомную массу до ближайшего целого числа.Атомная масса — среднее число изотопов конкретного элемента, обычно она не выражается целым числом
В нашем примере 190,23 округляется до 190.
5
Вычтите атомный номер из атомной массы. Поскольку абсолютная часть атомной массы приходится на протоны и нейтроны, вычитание числа протонов (то есть атомного номера, который равен числу протонов) из атомной массы дает число нейтронов в атоме. Цифры после десятичной запятой относятся к очень малой массе электронов в атоме. В нашем примере: 190 (атомный вес) — 76 (число протонов) = 114 (число нейтронов).
6
Запомните формулу. Чтобы найти число нейтронов в будущем, просто используйте эту формулу:
N = M – n
N = количество нейтронов
M = атомная масса
n = атомный номер
Метод 2 из 2:
Определение числа нейтронов в изотопах
-
1
Найдите элемент в периодической таблице. В качестве примера мы будем рассматривать изотоп углерода 14С. Поскольку неизотопный углерод 14С есть просто углерод С, найдите углерод в периодической таблице (второй период или второй ряд сверху).
-
2
Найдите атомный номер элемента. Это, как правило, наиболее заметное число в ячейке элемента и обычно находится над его символом (в варианте периодической системы, которую мы используем в нашем примере, других номеров и нет). Атомный номер – это количество протонов в одном атоме этого элемента. Углерод находится под номером 6, то есть один атом углерода имеет шесть протонов.
-
3
Найдите атомную массу. В случае изотопов делать это очень просто, так как они названы в соответствии с их атомной массой. В нашем случае у углерода 14С атомная масса равна 14. Теперь мы знаем атомную массу изотопа; последующий процесс расчета такой же, как и для определения числа нейтронов в атомах (не изотопах).
-
4
Вычтите атомный номер из атомной массы. Поскольку абсолютная часть атомной массы приходится на протоны и нейтроны, вычитание числа протонов (то есть атомного номера, который равен числу протонов) из атомной массы дает число нейтронов в атоме. В нашем примере: 14 (атомная масса) — 6 (число протонов) = 8 (число нейтронов).
-
5
Запомните формулу. Чтобы найти число нейтронов в будущем, просто используйте эту формулу:
-
N = M – n
- N = количество нейтронов
- M = атомная масса
- n = атомный номер
-
N = M – n
- Протоны и нейтроны составляют практически абсолютную массу элементов, в то время как электроны и прочие частицы составляют крайне незначительную массу (эта масса стремится к нулю). Так как один протон имеет примерно ту же массу, что и один нейтрон, а атомное число представляет собой число протонов, то можно просто вычесть число протонов от общей массы.
- Осмий — металл в твердом состоянии при комнатной температуре, получил свое название от греческого слова «osme» — запах.
- Если вы не уверены, что значит какое-то число в периодической таблице, запомните: таблица, как правило, строится вокруг атомного номера (то есть числа протонов), который начинается с 1 (водород) и растет на одну единицу слева направо, заканчиваясь на 118 (Оганесон). Это потому, что число протонов в атоме определяет сам элемент и такое число — наиболее легкий способ систематизации элементов (например, атом с 2 протонами — всегда гелий, так же, как и атом с 79 протонами — всегда золото).
8.
Мюон
Мюоны имеют такой же отрицательный заряд, как и электроны, но в 200 раз больше массы. Они возникают, когда частицы высокой энергии, называемые космическими лучами, врезаются в атомы в атмосфере Земли.
Путешествуя со скоростью, близкой к скорости света, мюоны осыпают Землю со всех сторон. Каждая область планеты размером с руку поражена примерно одним мюоном в секунду, и частицы могут пройти через сотни метров твердого материала, прежде чем они будут поглощены.
По словам Кристины Карлогану, физика из Физической лаборатории Клермон-Феррана во Франции, их вездесущность и проникающая способность делают мюоны идеальными для визуализации больших плотных объектов без их повреждения.
Физика8 класс
§ 29. Строение атомов
Атомы разных элементов в обычном состоянии отличаются друг от друга числом электронов, движущихся вокруг ядра. Так, в атоме водорода вокруг ядра движется один электрон, в атоме гелия — два электрона. Есть атомы с тремя, четырьмя электронами и т. д. Вокруг ядра атома кислорода движется 8 электронов, железа — 26, урана — 92 электрона.
Но всё же главной характеристикой данного химического элемента является не число электронов, а заряд ядра.
Дело в том, что электроны могут иногда отрываться от атома и тогда общий заряд электронов в атоме изменится. Заряд же ядра изменить очень трудно. А если он изменится, то получится уже другой химический элемент.
Так как заряд ядра равен по абсолютному значению общему заряду электронов атома, можно предположить, что в составе ядра находятся положительно заряженные частицы. Их назвали протонами. Масса протона 1,67•10-27 кг, что почти в 1840 раз больше, чем масса электрона.
Заряд протона положителен и равен по абсолютному значению заряду электрона.
Дальнейшее изучение состава ядра позволило предположить, что, кроме протонов, в ядрах атомов содержатся ещё нейтральные (не имеющие заряда) частицы. Они получили название нейтронов. Масса нейтрона не намного больше массы протона.
Итак, строение атома таково: в центре атома находится ядро, состоящее из протонов и нейтронов, а вокруг ядра движутся электроны.
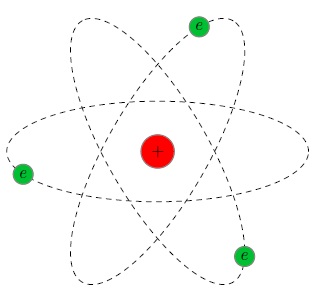
Рис. 40. Модели атомов:
а — водорода; б — гелия; в — лития
На рисунке 40 показаны модели атомов водорода (рис. 40, а), гелия (рис. 40, б) и лития (рис. 40, в). Протоны обозначены на рисунке кружками со знаком « + », нейтроны — серыми кружками (соотношение размеров и расстояний на рисунке не соблюдено).
Напомним, что атом в целом не имеет заряда, он нейтрален, потому что положительный заряд его ядра равен отрицательному заряду всех его электронов.
Но атом, потерявший один или несколько электронов, уже не является нейтральным, а будет иметь положительный заряд. Его называют тогда положительным ионом.
Наблюдается и обратное. Лишний электрон присоединяется к нейтральному атому. В этом случае атом приобретает отрицательный заряд и становится отрицательным ионом.
Вопросы
- Чем отличаются друг от друга атомы различных химических элементов?
- Что является главной характеристикой данного химического элемента?
- Какие частицы входят в состав ядра?
- Каково строение атомов водорода, гелия и лития?
- Как образуются положительные и отрицательные ионы?
Упражнение 20
- В ядре атома углерода содержится 12 частиц. Вокруг ядра движутся 6 электронов. Сколько в ядре этого атома протонов и сколько нейтронов?
- От атома гелия отделился один электрон. Как называется оставшаяся частица? Каков её заряд?
- Существуют ли атомы с зарядом ядра меньшим, чем заряд протона?
Как выглядят атомные частицы?
Наиболее крупными атомными частицами считаются протоны и нейтроны, которые несколько тяжелее электронов и располагаются прямо в самом центре атома. Электроны же образуют легковесное облако, которое вращается вокруг атомного ядра. Известно, что вес 1800 электронов соответствует одному тяжеловесу-протону. Помимо этого, добавление хотя бы одного протона к атому приводит к образованию нового вещества с отличными от оригинала свойствами, причем добавление лишнего нейтрона создает всего лишь изотоп вещества или же просто более тяжелую его версию.
Ядро атома состоит из протонов, нейтронов и электронов, которые, в свою очередь, состоят из кварков
Наиболее крупными атомными частицами считаются протоны и нейтроны, которые несколько тяжелее электронов и располагаются прямо в самом центре атома. Электроны же образуют легковесное облако, которое вращается вокруг атомного ядра. Известно, что вес 1800 электронов соответствует одному тяжеловесу-протону. Помимо этого, добавление хотя бы одного протона к атому приводит к образованию нового вещества с отличными от оригинала свойствами, причем добавление лишнего нейтрона создает всего лишь изотоп вещества или же просто более тяжелую его версию.
Как уже говорилось выше, абсолютно все элементарные частицы состоят из кварков. которые представляют из себя основу мироздания. Интересный факт: Название “кварк” было взято в одном из романов известного в XX веке писателя-модерниста Джеймса Джойса, который необычным словом решил обозначить звук, воспроизводимый утками.
Джеймс Джойс — писатель, благодаря которому появился термин «кварки»
Сами же кварки подразделяются на 6 так называемых “ароматов”, каждый из которых обладает своими собственными характеристиками или “цветом”. Кроме того, каждый из 6 типов кварков обладает и собственным весьма оригинальным именем. Так, помимо нижнего и верхнего видов кварков, существуют также странный, очарованный, прелестный и истинный кварки.
Конечно же, “странность” или “прелестность” кварков сильно отличаются от привычных нам понятий. Точно так же, как и понятие цвета кварков на самом деле имеет в виду далеко не их оттенок, но способ взаимодействия кварков и других микрочастиц — глюонов. Что ж, фантазия ученых иногда умеет удивлять.
В любом случае, кварки представляют из себя по-настоящему уникальные частицы, от которых во всех смыслах зависит существование нашей Вселенной в том виде, в котором мы ее знаем. Быть может, тайна возникновения Большого взрыва и наше постижение основных законов Вселенной действительно зависят от одной крошечной песчинки, которая в тысячи и тысячи раз меньше атома.
Базовая модель атома и атомная теория
Все вещества состоят из частиц, называемых атомами. Атомы связываются друг с другом, образуя элементы, и содержат только один вид атома.
Атомы различных элементов образуют соединения, молекулы и объекты.
Атом — это строительный блок материи, который нельзя разбить на части с помощью каких-либо химических средств.
Ядерные реакции могут изменить атомы.
Три части атома — это протоны (положительно заряженные), нейтроны (нейтральный заряд) и электроны (отрицательно заряженные).
Протоны и нейтроны образуют атомное ядро.
Электроны притягиваются к протонам в ядре, но движутся так быстро, что падают к нему (орбите), а не прилипают к протонам.
Идентичность атома определяется его числом протонов. Это также называется его атомным номером.
Части Атома
Атомы состоят из трех частей:
Протоны: протоны являются основой атомов. В то время как атом может получать или терять нейтроны и электроны, его идентичность связана с числом протонов. Символом числа протонов является заглавная буква Z.
Нейтроны: число нейтронов в атоме обозначается буквой N. Атомная масса атома является суммой его протонов и нейтронов или Z + N. Сильная ядерная сила связывает протоны и нейтроны вместе, образуя ядро атом.
Электроны: электроны намного меньше протонов или нейтронов и вращаются вокруг них.
Основные характеристики атомов:
Атомы не могут быть разделены с помощью химических веществ. Они состоят из частей, которые включают протоны, нейтроны и электроны, но атом является основным химическим строительным материалом материи. Ядерные реакции, такие как радиоактивный распад и деление, могут разрушать атомы.
Каждый электрон имеет отрицательный электрический заряд.
Каждый протон имеет положительный электрический заряд. Заряд протона и электрона равен по величине, но противоположен по знаку. Электроны и протоны электрически притягиваются друг к другу. Как заряды (протоны и протоны, электроны и электроны) отталкиваются друг от друга.
Каждый нейтрон электрически нейтрален; иными словами, нейтроны не имеют заряда и не притягиваются электрически ни к электронам, ни к протонам.
Протоны и нейтроны имеют примерно одинаковые размеры и намного больше электронов. Масса протона по существу такая же, как у нейтрона.
Масса протона в 1840 (!) раз больше массы электрона.
Ядро атома содержит протоны и нейтроны. Ядро несет положительный электрический заряд.
Электроны движутся вне ядра; они организованы в оболочки, которые являются областью наиболее вероятного их местонахождения.
Простые модели показывают, что электроны вращаются вокруг ядра по почти круговой орбите, подобно планетам, вращающимся вокруг звезды, но реальное поведение намного сложнее.
Некоторые электронные оболочки напоминают сферы, но другие больше похожи на тупые колокольчики или другие формы.
Технически, электрон может быть найден в любом месте в пределах атома, но проводит большую часть своего времени в области, описываемой орбиталью.
Электроны также могут перемещаться между орбиталями.
Атомы очень маленькие. Средний размер атома составляет около 100 пикометров или одну десятитысячную часть метра.
Почти вся масса атома находится в его ядре; почти весь объем атома занят электронами.
Количество протонов (также известно как его атомный номер) определяет элемент.
Изменение количества нейтронов приводит к образованию изотопов. Изменение числа электронов приводит к образованию ионов. Изотопы и ионы атома с постоянным числом протонов — это вариации одного элемента.
Частицы внутри атома связаны друг с другом мощными силами.
В общем, электроны легче добавлять или удалять из атома, чем протон или нейтрон.
Химические реакции в основном включают атомы или группы атомов и взаимодействия между их электронами.
Ядро атома. Изотопы
Атом состоит из ядра, которое имеет положительный заряд, и электронов, которые имеют отрицательный заряд. В целом атом электронейтрален.
Положительный заряд ядра атома равен порядковому номеру химического элемента.
Ядро атома — сложная частица. В ней сосредоточена почти вся масса атома. Поскольку химический элемент — совокупность атомов с одинаковым зарядом ядра, то около символа элемента указывают (рис. 6).
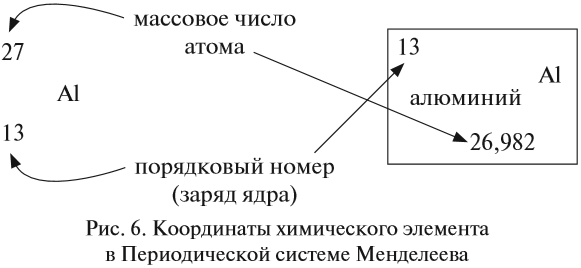
По этим данным можно определить состав ядра. Ядро состоит из протонов и нейтронов.
- Протон (р) имеет массу, равную 1 (1,0073 а. е. м.) и заряд, равный +1.
- Нейтрон (n) заряда не имеет (нейтрален), а масса его приблизительно равна массе протона (1,0087 а. е. м.).
Какие частицы определяют заряд ядра? Протоны! Причём число протонов равно (по величине) заряду ядра атома, т. е. порядковому номеру:
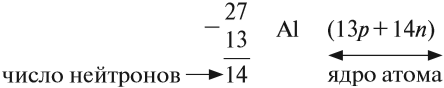
Число нейтронов определяют по разности между величинами: «масса ядра» и «порядковый номер».
Задание 3.3. Определите состав ядер атомов, если химический элемент находится в:
- 3-м периоде, VII группе, главной подгруппе;
- 4-м периоде, IV группе, побочной подгруппе;
- 5-м периоде, I группе, главной подгруппе.
Обратите внимание, что при определении массового числа ядра атома приходится округлять атомную массу, указанную в Периодической системе! Почему? Ведь массы протона и нейтрона практически целочисленны, а массой электронов можно пренебречь. Для того,чтобы ответить на этот вопрос, нужно понять:
Для того,чтобы ответить на этот вопрос, нужно понять:
- Что происходит с атомом в ходе химических процессов;
- Что такое «химический элемент».
В химических процессах обязательно изменяется распределение электронов вокруг ядра или даже изменяется их число. В последнем случае атом отдаёт или принимает электроны и превращается в заряженную частицу — ион. Но в химических реакциях никогда не меняется состав ядра атома, его заряд. Поэтому заряд ядра атома является своеобразным «паспортом» химического элемента.
Химический элемент — совокупность атомов или ионов с одинаковым зарядом ядра.
Для того чтобы разобраться, попробуйте определить, какие из ядер, состав которых указан ниже, принадлежат одному и тому же химическому элементу:
Атомам одного химического элемента принадлежат ядра А и В, так как они содержат одинаковое число протонов, т. е. заряд этих ядер одинаковый. Но ведь у них разная масса! Исследования показывают, что масса атома не оказывает существенного влияния на его химические свойства. Поэтому атомы одного и того же химического элемента (одинаковое число протонов), но с разной массой (разное число нейтронов) являются ИЗОТОПАМИ* этого элемента.
В таблице Менделеева указана средняя атомная масса всех природных изотопов данного элемента (Аr). Изотопы и их химические соединения отличаются друг от друга по физическим свойствам, но химические свойства у изотопов одного химического элемента одинаковы. Так, изотоп углерода-14 (14С) имеет такие же химические свойства, как и углерод-12 (12С), который входит в ткани любого живого организма, отличаясь от него только радиоактивностью. Поэтому изотопы применяют для диагностики и лечения различных заболеваний, для научных исследований.
Элемент «водород» встречается в природе в виде трёх изотопов:
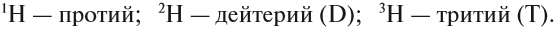
Химический элемент «кислород» также представлен тремя природными изотопами:
Задание 3.4. Укажите состав ядер этих изотопов водорода и кислорода.
Если разные вещества содержат атомы одного и того же химического элемента, это не означает, что эти вещества имеют одни те же свойства. Например, химический элемент «хлор» в виде атомарного хлора Cl• разрушает метан, а также атмосферный озон. Тот же элемент в виде молекулярного хлора Cl2 ядовит, активно реагирует с водой, многими металлами, а ионы хлора (химический элемент — тот же!) в составе NaCl химически инертен, а с биологической точки зрения не только безвреден, но и полезен для нас. Эти ионы являются макроэлементами нашей пищи, которые входят в состав крови, желудочного сока. Суточная потребность — до 6 граммов.
Но вернемся к описанию строения атома.

10.
Бозон Хиггса
Физике частиц обычно тяжело конкурировать с политикой и сплетнями знаменитостей за заголовки, но бозон Хиггса привлек серьезное внимание. Возможно, знаменитое и неоднозначное прозвище знаменитого бозона, «Частица Бога», заставляло гудеть средства массовой информации.
С другой стороны, интригующая возможность того, что бозон Хиггса отвечает за всю массу во Вселенной, захватывает воображение.
Бозон Хиггса является, если не сказать, самой дорогой частицей всех времен
Это немного несправедливое сравнение; например, для открытия электрона потребовалось немного больше, чем для вакуумной трубки и настоящего гения, а для поиска бозона Хиггса потребовалось создание экспериментальных энергий, которые раньше редко встречались на планете Земля.
Наука и технологии
3 июня, 2020
206 просмотров
Когда происходит подобное? Из-за чего атомы могут, например, терять электроны?
Это бывает при высоких температурах, то есть тогда, когда атомы газа имеют большую энергию и скорости, носятся, как сумасшедшие, сталкиваются друг с другом. Мы ведь с вами помним, что частота и скорость соударений и есть температура. В обычном воздухе скорость соударений молекул невелика. А вот на Солнце раскаленный газ имеет температуру в тысячи (на поверхности Солнца) и даже десятки миллионов градусов (внутри нашего светила). Я сказал «на Солнце»? Это немного неточно. Скорее, «в Солнце». Потому что Солнце представляет собой раскаленный газовый шар. В основном оно состоит из водорода с небольшой примесью гелия.
Так вот в этих условиях скорость соударения атомов водорода такова, что «крышу срывает» у атомов на всю катушку. Атомы разрушаются, электроны слетают со своих орбит и начинают метаться одни, так же, как и протоны. Получается хаотическая электронно-протонная смесь или, иначе говоря, ионизированная плазма.
Плазма – горячая смесь ионов. Огонь – это тоже плазма. Только в обычном пламени костра или свечи содержание ионов не такое большое, как на Солнце, потому что температура ниже.
Я загрузил вас новыми словами – «ионы», «плазма». Но зато теперь вы можете похвастаться тем, что знаете целых четыре состояния вещества!
Первое – твердое. Атомы и молекулы в таком веществе крепко держатся друг за друга, никуда не бегают, а только чуть-чуть дрожат и топчутся на одном месте, образуя кристаллическую решетку.
Второе состояние вещества – жидкое. Здесь уже энергетика частичек вещества такова, что они ломают кристаллическую структуру, рушат тесные ряды и начинают хаотически бродить, будучи не в силах удержаться в твердой структуре. Растекаются. Но еще не разлетаются друг от друга.
Разлетаться они начнут в третьем состоянии вещества – газообразном, которое наступит при дальнейшем нагреве, то есть дальнейшей накачке вещества энергией. Тогда скорость атомов станет уже такой, что силы их притяжения не смогут сдерживать энергичность расшалившихся атомов. Они просто разлетятся друг от друга и рассеются в пространстве.
Если же газ собрать в каком-то закрытом объеме или просто удерживать мощной силой гравитации (как на Солнце) и продолжать нагревать, то энергетика атомов станет уже такой огромной, что при столкновении друг с другом будут разрушаться уже сами атомы – с них начнет срывать электронные шубы. И останутся только ионы, ионизированный газ – плазма. При этом газ начнет светиться, что говорит о его высокой температуре.
Плазма – это прекрасно. Мы любим смотреть на плазму…